Методы развития творчества в предметной деятельности школьников достаточно многообразны. В развивающем курсе «Основы химии для начальной школы» [10], реализуемом в лицее № 130 города Екатеринбурга, применяется технология решения экспериментальных творческих задач по химии для формирования опыта химического творчества младших школьников, с обретения которого начинается развитие чувства вещества.
Чувство вещества – это точное восприятие внешних свойств (цвета, запаха, вкуса, дисперсности) веществ и их изменений, происходящих при химических реакциях, развитые кинестезические ощущения, глазомерная оценка массы и объема, ощущение времени и пространства, в которых совершаются химические превращения веществ, понимание связи между составом вещества, его свойствами и нахождением в Природе. [7] На основе развитого чувства вещества формируется ответственное и нравственное поведение при взаимодействии с химическими веществами.
Чувство вещества как метапредметный результат обучения химии формируется в деятельности множественного решения экспериментальных химических задач, их критического осмысления, расширения области поиска решений, «не зацикливания» на первой пришедшей в голову идее, освобождения от стереотипных установок в процессе генерирования идей и (ключевой момент творческого процесса) нахождения интуитивного решения. Адаптированные методы научного творчества системы НФТМ-ТРИЗ [8] являются эффективным педагогическим инструментом конструирования развивающего пространства реализации такой деятельности, элементарным обучающим модулем которого является креативное занятие.
Креативное занятие состоит из специально продуманной системы эвристических заданий [3, 4, 5, 6], активизирующих познавательный интерес и «подпитывающих» мотивацию «к учению» в ходе всего занятия, предусматривает чередование видов деятельности, психологические разгрузки и рефлексию. Каждый блок занятия реализует свои задачи и имеет оригинальное содержание.
Чувство вещества как метапредметный результат обучения химии формируется в деятельности множественного решения экспериментальных химических задач, их критического осмысления, расширения области поиска решений, «не зацикливания» на первой пришедшей в голову идее, освобождения от стереотипных установок в процессе генерирования идей и (ключевой момент творческого процесса) нахождения интуитивного решения. Адаптированные методы научного творчества системы НФТМ-ТРИЗ [8] являются эффективным педагогическим инструментом конструирования развивающего пространства реализации такой деятельности, элементарным обучающим модулем которого является креативное занятие.
Креативное занятие состоит из специально продуманной системы эвристических заданий [3, 4, 5, 6], активизирующих познавательный интерес и «подпитывающих» мотивацию «к учению» в ходе всего занятия, предусматривает чередование видов деятельности, психологические разгрузки и рефлексию. Каждый блок занятия реализует свои задачи и имеет оригинальное содержание.
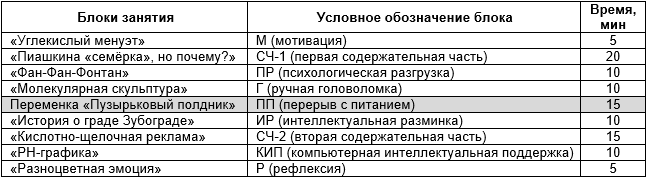
Таблица 1
Информационная карта креативного занятия [12]
по программе «Основы химии для начальной школы», 4 класс
Блоки занятия Условное обозначение блока Время,
мин
«Углекислый менуэт М (мотивация) 5
«Пиашкина «семёрка», но почему?» СЧ-1 (первая содержательная часть) 20
«Фан-Фан-Фонтан» ПР (психологическая разгрузка) 10
«Молекулярная скульптура» Г (ручная головоломка) 10
Переменка «Пузырьковый полдник» ПП (перерыв с питанием) 15
«История о граде Зубограде» ИР (интеллектуальная разминка) 10
«Кислотно-щелочная реклама» СЧ-2 (вторая содержательная часть) 15
«PH-графика» КИП (компьютерная интеллектуальная поддержка) 10
«Разноцветная эмоция» Р (рефлексия) 5
мин
«Углекислый менуэт М (мотивация) 5
«Пиашкина «семёрка», но почему?» СЧ-1 (первая содержательная часть) 20
«Фан-Фан-Фонтан» ПР (психологическая разгрузка) 10
«Молекулярная скульптура» Г (ручная головоломка) 10
Переменка «Пузырьковый полдник» ПП (перерыв с питанием) 15
«История о граде Зубограде» ИР (интеллектуальная разминка) 10
«Кислотно-щелочная реклама» СЧ-2 (вторая содержательная часть) 15
«PH-графика» КИП (компьютерная интеллектуальная поддержка) 10
«Разноцветная эмоция» Р (рефлексия) 5
1. Блок «Углекислый менуэт» (М). Комментарий для учителя: Данный блок представляет собой систему демонстрационных опытов, иллюстрирующих способность угольной кислоты в составе газированных напитков разрушать карбонатные и фосфатные соли скорлупы яйца и кости. Демонстрируется опыт «Танцующая шоколадка» [1] и результаты опытов «Голое яйцо» и «Резиновая кость» [9]. Комментарий для учащихся: В опытах, которые вы сейчас увидели, использована газированная вода. Скажите, какие вещества обнаруживаются легко и сразу при открывании бутылки с «газировкой»? (контрольный ответ (далее КО): вода и газ, этимологический анализ словосочетания «газированная вода»). Именно давление газа (мы еще вернемся к вопросу: какого газа?) заставляет шоколадку двигаться в растворе! Но! Из-за чего исчезла яичная «одежка»? Почему кость «превратилась» шланг? Секрет этих наблюдаемых изменений в свойствах невидимого в газированном напитке вещества, название которого … разгадайте ребус.
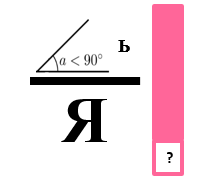
Рис. 1. Эвристическое задание 1. Ребус «УГОЛЬНАЯ КИСЛОТА»
Итак, это угольная кислота. И теперь понятно, какой же газ выделяется из «газировки»? (КО: углекислый газ, этимологический анализ словосочетания «угольная кислота»). Напоминаю, что при проведении опытов в химической лаборатории вещества (даже если это пищевые продукты!) нельзя брать руками и пробовать на вкус.
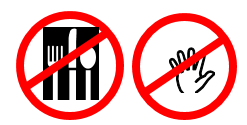
Рис. 2. Знаки техники безопасности: «Нельзя пробовать на вкус!» и «Нельзя трогать руками!»
2. Блок «Пиашкина «семёрка», но почему?» (СЧ-1). Комментарий для учителя: Этот блок содержит программный материал урока по темам «Задачка о верблюжьем спирте и муравьином яде» и «Задачка об угольной кислоте и яичной скорлупе» развивающего курса «Основы химии» для 4 класса [10], насыщен эвристическими заданиями на развитие творческого воображения и химическими опытами, демонстрирующими процессы нейтрализации в растворах кислот и щелочей, в том числе, с участием угольной кислоты. Комментарий для учащихся: Итак, наши наблюдения и разгадка ребуса позволяют нам предположить, что в цилиндре находится смесь воды, углекислого газа и угольной кислоты, именно эта смесь является основой газированных напитков. Угольная кислота образуется при растворении углекислого газа в воде под высоким давлением. Рассмотрите схему образования угольной кислоты.
2. Блок «Пиашкина «семёрка», но почему?» (СЧ-1). Комментарий для учителя: Этот блок содержит программный материал урока по темам «Задачка о верблюжьем спирте и муравьином яде» и «Задачка об угольной кислоте и яичной скорлупе» развивающего курса «Основы химии» для 4 класса [10], насыщен эвристическими заданиями на развитие творческого воображения и химическими опытами, демонстрирующими процессы нейтрализации в растворах кислот и щелочей, в том числе, с участием угольной кислоты. Комментарий для учащихся: Итак, наши наблюдения и разгадка ребуса позволяют нам предположить, что в цилиндре находится смесь воды, углекислого газа и угольной кислоты, именно эта смесь является основой газированных напитков. Угольная кислота образуется при растворении углекислого газа в воде под высоким давлением. Рассмотрите схему образования угольной кислоты.

Рис. 3. Схема образования угольной кислоты
Назовите, по меньшей мере, два признака, по которым можно доказать, что в растворе есть кислота (КО: 1) у раствора должен быть кислый вкус, 2) индикатор должен показать кислую «погоду»-среду). Рассмотрите «напоминалки».
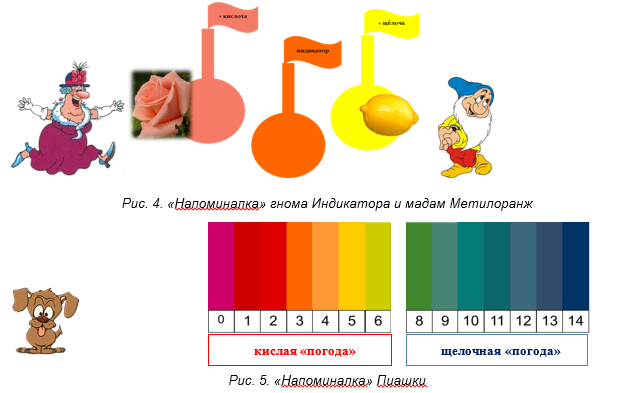
Какая «полоска» исчезла из Пиашкиной «напоминалки»? Какой «погоде»-среде в растворе соответствует Пиашкино число 7? Какой «погоде»-среде в растворе соответствует оранжевый цвет раствора в «напоминалке» гнома Индикатора и мадам Метилоранж?
Эвристическое задание 2. Прочтите отрывок из стихотворения поэтессы Беллы Ахмадулиной «Газированная вода» [2]:
Воспрянув из серебряных оков,
родится омут сладкий и соленый,
неведомым дыханьем населенный
и свежей толчеею пузырьков.
Все радуги, возникшие из них,
пронзают небо в сладости короткой,
и вот уже, разнеженный щекоткой,
семь вкусов спектра пробует язык.
Проанализируйте эти строки, сопоставьте со своим личным жизненным опытом и ответьте на вопрос: есть ли кислый вкус у газированной минеральной воды или, например, напитков марки «Пепси-кола»? А у напитков марки «Фанта»? Как вы думаете, почему в последнем случае у раствора кислый вкус? Как вы думаете, связан ли факт наличия кислого вкуса с присутствием угольной кислоты в газированных растворах? Таким образом, установлено (вставьте пропущенное слово): ГАЗИРОВАННЫЕ РАСТВОРЫ БЕЗ ВКУСОВЫХ ДОБАВОК КИСЛЫМ ВКУСОМ … (КО: не обладают). А теперь решим экспериментальную задачку.
Экспериментальная задачка № 1. В пяти ячейках пластины для капельных реакций находятся образцы газированной воды разных торговых марок (номер ячейки – номер образца в таблице 2), определите «погоду»-среду в каждом растворе с помощью универсального индикатора и раствора метилового оранжевого, для каждой пробы укажите Пиашкино число. Результаты исследования отметьте в листике-отчётике.
Таблица 2

Таким образом, установлено (вставьте пропущенное слово): «ПОГОДА»-СРЕДА В ГАЗИРОВАННЫХ РАСТВОРАХ … (нейтральная).
ОДНАКО, УГОЛЬНАЯ КИСЛОТА В ГАЗИРОВАННЫХ РАСТВОРАХ ЕСТЬ, А ПРИЗНАКОВ ЕЁ НАЛИЧИЯ НЕ ОБНАРУЖЕНО. Для разрешения этого противоречия выполним несколько заданий.
Эвристическое задание 3. Предположите характер «погоды»-среды в водных растворах знакомых веществ. Подсказка: из выбранных букв составится название «газировкиной» кислоты (УГОЛЬНАЯ).
ОДНАКО, УГОЛЬНАЯ КИСЛОТА В ГАЗИРОВАННЫХ РАСТВОРАХ ЕСТЬ, А ПРИЗНАКОВ ЕЁ НАЛИЧИЯ НЕ ОБНАРУЖЕНО. Для разрешения этого противоречия выполним несколько заданий.
Эвристическое задание 3. Предположите характер «погоды»-среды в водных растворах знакомых веществ. Подсказка: из выбранных букв составится название «газировкиной» кислоты (УГОЛЬНАЯ).
Таблица 3
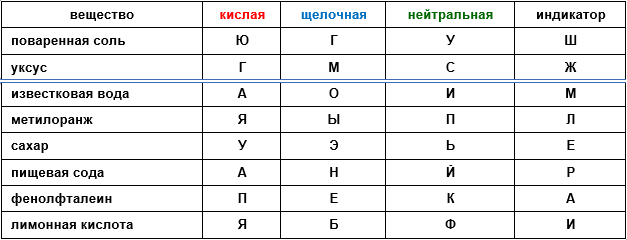

Экспериментальная задачка №2. В ячейках пластины для капельных реакций находятся водные растворы, соответственно, в 1 – уксусной кислоты; во 2 – лимонной кислоты; в 3 – пищевой соды; добавьте в 1 и 2 пробы по 2 капли раствора метилового оранжевого и убедитесь в кислой реакции растворов; затем в каждую пробу по каплям добавляйте раствор пробы 3. Почему исчезает окраска цвета «чайной розы»? Какая остаточная окраска у обоих растворов? Какой «погоде» в растворе она соответствует? Какую окраску приобретут растворы 1, 2 при дополнительном добавлении раствора пробы 3? Какой «погоде» в растворе она соответствует?
Эвристическое задание 4. Используя вместо X и Y названия веществ из таблицы 3, составьте верное равенство:
Х + Y = НЕЙТРАЛЬНАЯ «ПОГОДА»-СРЕДА
Рассмотрите все возможные варианты Х и Y. Помните: в данном случае, в химии, как в математике от перемены мест слагаемых сумма не меняется (КО: уксус + пищевая сода; уксус + известковая вода или наоборот; лимонная кислота + пищевая сода; лимонная кислота + известковая вода или наоборот).
Таким образом, установлено: нейтральная «погода»-среда в растворе образуется при добавлении к кислоте щелочи или наоборот. Этот процесс называется нейтрализацией. Рассмотрите схему нейтрализации:
Эвристическое задание 4. Используя вместо X и Y названия веществ из таблицы 3, составьте верное равенство:
Х + Y = НЕЙТРАЛЬНАЯ «ПОГОДА»-СРЕДА
Рассмотрите все возможные варианты Х и Y. Помните: в данном случае, в химии, как в математике от перемены мест слагаемых сумма не меняется (КО: уксус + пищевая сода; уксус + известковая вода или наоборот; лимонная кислота + пищевая сода; лимонная кислота + известковая вода или наоборот).
Таким образом, установлено: нейтральная «погода»-среда в растворе образуется при добавлении к кислоте щелочи или наоборот. Этот процесс называется нейтрализацией. Рассмотрите схему нейтрализации:
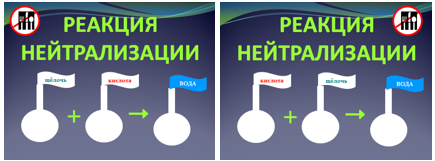
Рис. 6. Схема нейтрализации.
Но в газированную воду (раствор угольной кислоты) мы щелочь НЕ добавляли, почему же реакция раствора – нейтральная? Объясняется этот факт таким образом: угольная кислота – неустойчива и разлагается в растворе с образованием воды и углекислого газа, который частично улетает из раствора, а частично снова растворяется, образуя угольную кислоту уже в меньшем количестве, поэтому кислотность раствора очень маленькая, её «не чувствует кислой» ни наш язык (хотя угольная кислота точечно щиплется и щекочет нос), ни химический индикатор. Такой процесс можно условно назвать самонейтрализацией. Рассмотрите схему самонейтрализации:

Рис. 7. Схема самонейтрализации

Рис. 7. Схема самонейтрализации
3. Блок «Фан-Фан-Фонтан» (ПР). Комментарий для учителя: Выполнение зрелищного опыта «Фонтан из газировки», освежающего и пахучего, ослабляет умственное и нервное напряжения. Учащиеся объединяются в группы по 3-4 участника вокруг столов, на которых находятся наборы для проведения опытов: «Кола-фонтан», «Спрайт-фонтан», «Минеральный фонтан», в набор входит соответствующий названию газированный напиток в закупоренной бутылочке (чем больше емкость бутылочки, тем эффектнее результат) и по 5-10 драже «Ментос». Демонстрация опыта осуществляется последовательно каждой группой и наблюдается всеми учащимися. Комментарий для учащихся: Выполните опыт, для этого откройте бутылочку газированного напитка, быстро опустите в неё драже «Ментос», быстро чуть-чуть прикрутите крышку, выдержите 1-2 секунды, резко откройте крышку и наблюдайте результат. «Выброс» фонтанов можно приветствовать хлопками и речитативом: «Ментос» бросим в газировку и закроем крышку ловко! Посчитаем: раз-два … ай! Фонтан скорее выпускай!»
4. Блок «Молекулярная скульптура» (Г). Комментарий для учителя: Учащиеся получают набор для пространственного моделирования молекул, осуществляют сборку модели молекулы угольной кислоты, а также её перестройку с образованием моделей молекул воды и углекислого газа, что иллюстрирует реакцию разложения угольной кислоты в растворе. Комментарий для учащихся: Нужно собрать модель молекулы угольной кислоты, учитывая валентности образующих её атомов, затем перестроить модель так, чтобы получились модели молекул воды и углекислого газа, из которых образуется угольная кислота в растворе и на которые частично распадается при самонейтрализации. Перед построением модели рассмотрите «напоминалку» Табу Валентности.
4. Блок «Молекулярная скульптура» (Г). Комментарий для учителя: Учащиеся получают набор для пространственного моделирования молекул, осуществляют сборку модели молекулы угольной кислоты, а также её перестройку с образованием моделей молекул воды и углекислого газа, что иллюстрирует реакцию разложения угольной кислоты в растворе. Комментарий для учащихся: Нужно собрать модель молекулы угольной кислоты, учитывая валентности образующих её атомов, затем перестроить модель так, чтобы получились модели молекул воды и углекислого газа, из которых образуется угольная кислота в растворе и на которые частично распадается при самонейтрализации. Перед построением модели рассмотрите «напоминалку» Табу Валентности.
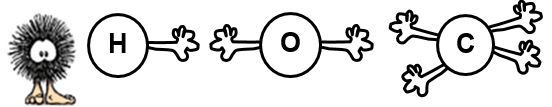
Рис. 8. «Напоминалка» Табу Валентности.
Переменка «Пузырьковый полдник». Комментарий для учителя: Это необходимый перерыв после 40 минут первой части занятия, совмещённый полдником, в составе полдника рекомендовано употребление газированной минеральной воды или кислородного коктейля.
5. Блок «История о граде Зубограде» (ИР). Комментарий для учителя: Этот блок содержит творческое задание: закончить необычную историю с химическим сюжетом, в ходе выполнения задания дети актуализируют личностный опыт творческого воображения и фантазирования, что настраивает их на продуктивную работу во второй части занятия. Комментарий для учащихся: Наши наблюдения (опыты в начале урока) подтверждают, что кислоты разрушительны для яичной скорлупы, которая состоит в основном из карбоната кальция, и куриной кости, имеющей фосфатную основу. Значит, кислоты разрушают карбонаты и фосфаты. Но зубная эмаль также состоит из фосфатных солей, об этом наша история.
Эвристическое задание 5. Послушайте начало истории, а затем придумайте её «научное» продолжение.
5. Блок «История о граде Зубограде» (ИР). Комментарий для учителя: Этот блок содержит творческое задание: закончить необычную историю с химическим сюжетом, в ходе выполнения задания дети актуализируют личностный опыт творческого воображения и фантазирования, что настраивает их на продуктивную работу во второй части занятия. Комментарий для учащихся: Наши наблюдения (опыты в начале урока) подтверждают, что кислоты разрушительны для яичной скорлупы, которая состоит в основном из карбоната кальция, и куриной кости, имеющей фосфатную основу. Значит, кислоты разрушают карбонаты и фосфаты. Но зубная эмаль также состоит из фосфатных солей, об этом наша история.
Эвристическое задание 5. Послушайте начало истории, а затем придумайте её «научное» продолжение.

Рис. 9. Иллюстрации к «Истории о граде Зубограде»
«Жили-были в Великом Граде Зубограде малыш Тридцать Второй Зуб и его многочисленные белые братья, тоже Зубы. Однажды в их городе прошёл Кислотный Дождь. Страшное разрушение принёс он Зубограду. Но настоящая беда нагрянула, когда заглянул к ним проездом из города Языкобурга Барбариска Микроб. Расплодился он и размножился по улицам Зубограда, да ещё дружка своего пригласил – Кариеса Разрушителя-Вонючку. И позвали белые братья Зубы на подмогу …» (Один из интересных ответов с загадкой (автор Андрей Войцык, 4в класс, 2013 год): «… соседей из страны Жвастиков и их мудрую правительницу Пасту Зубную Великолепную. И разразилась битва нешуточная: бурлили щелочные реки, вскипали кислотные берега, густели углекислые тучи. Барбариска Микроб, Вонючка-Кариес и их сподвижники трусливо бежали. А в городе Зубограде наступила КАПИТУЛЯЦИЯ. Какое слово я заменил на КАПИТУЛЯЦИЯ?» (КО: НЕЙТРАЛИЗАЦИЯ).
6. Блок «Кислотно-щелочная реклама» (СЧ-2). Комментарий для учителя: Этот блок логически связан с первой содержательной частью программного материала, но предполагает умение решать более сложные эвристические задания с целью применения личного опыта химического творчества в измененных условиях. Комментарий для учащихся: Итак, кислоты разрушают зубную эмаль, но известно немало способов защиты зубов от кислот. Давайте проанализируем способы, которые упоминаются в придуманных вами окончаниях «Истории о граде Зубограде», а также в известных рекламах. Можно ли жителям Зубограда (молочным и коренным) использовать жевательную резинку, чтобы отныне и впредь спасти свой город от разрушения? Почему полоскание рта после еды стало национальной традицией для всех поколений братьев Зубов со времен последней капитуляции-нейтрализации в городе Зубограде?
Эвристическое задание 6. «Каждый раз во время еды вы подвергаете свои зубы воздействию бактерий, вырабатывающих кислоту» – с этого утверждения начинается реклама одной из жевательных резинок. Какая ошибка содержится в этом тексте? (КО: Бактерии, вырабатывающие кислоту, постоянно присутствуют в полости рта, наши зубы постоянно подвергаются воздействию этих бактерий, а не только во время еды. А «каждый раз во время еды», мы поставляем этим бактериям углеводы, то есть дополнительное сырье, необходимое им для вырабатывания кислоты, поэтому во время еды разрушительное действие бактерий усиливается [11].
Экспериментальная задачка №3. Зубная паста «Blend-a-med», содержащая фтористые соли, – одна из самых рекламируемых, для демонстрации её укрепляющих зубную эмаль свойств показывают впечатляющий опыт с куриным яйцом, которое после обработки этой зубной пастой не растворяется даже в уксусной кислоте. Проверьте экспериментально правдивость этой рекламы [11].
Как вы думаете, почему скорлупа половинки яйца, обработанной зубной пастой «Blend-a-med», не растворяется в уксусной кислоте? (КО: от растворения скорлупу яйца (карбонат кальция) защищает образовавшаяся на поверхности скорлупы пленка фторида кальция) Какими известными вам веществами можно защитить скорлупу яйца от «кислотного удара»? (интересные ответы: обмазать силикатным клеем, покрыть лаком для ногтей, окунуть половинку яйца в расплавленный парафин, натереть салом или мазутом).
Эвристическое задание 7. Установите последовательность слов и словосочетаний в логике: «причина – плохое следствие – «спаситель» – хорошее следствие – результат»
а) кислая среда, смородина, «Дирол», аскорбиновая кислота, нейтрализация, слюна (КО: 2,4, 1,3, 6, 5); б) «Лесной бальзам», pH=7, пирожное, молочная кислота, pH=3, углеводы (КО: 3, 6, 4, 5, 1, 2).
7. Блок «pH-графика» (КИП). Комментарий для учителя: Блок компьютерной интеллектуальной поддержки позволяет использовать для решения задач дополнительные возможности компьютерной среды, в том числе, приборы цифровой химической лаборатории, осуществление учащимися разных форм мыслительных операций на внутреннем плане способствует развитию абстрактного воображения. Комментарий для учащихся: Вам нужно пересесть за компьютерные столы. Первое задание: с помощью учителя ознакомиться с принципом работы цифрового pH-метра и провести контрольное измерение pH дистиллированной воды. Второе задание: осуществить несколько последовательных измерений значения pH раствора при протекании реакции нейтрализации сока лимона раствором «Lacalut»; сделать качественный анализ полученного графика: как изменяется «погода»-среда в исследуемом растворе в ходе реакции.
6. Блок «Кислотно-щелочная реклама» (СЧ-2). Комментарий для учителя: Этот блок логически связан с первой содержательной частью программного материала, но предполагает умение решать более сложные эвристические задания с целью применения личного опыта химического творчества в измененных условиях. Комментарий для учащихся: Итак, кислоты разрушают зубную эмаль, но известно немало способов защиты зубов от кислот. Давайте проанализируем способы, которые упоминаются в придуманных вами окончаниях «Истории о граде Зубограде», а также в известных рекламах. Можно ли жителям Зубограда (молочным и коренным) использовать жевательную резинку, чтобы отныне и впредь спасти свой город от разрушения? Почему полоскание рта после еды стало национальной традицией для всех поколений братьев Зубов со времен последней капитуляции-нейтрализации в городе Зубограде?
Эвристическое задание 6. «Каждый раз во время еды вы подвергаете свои зубы воздействию бактерий, вырабатывающих кислоту» – с этого утверждения начинается реклама одной из жевательных резинок. Какая ошибка содержится в этом тексте? (КО: Бактерии, вырабатывающие кислоту, постоянно присутствуют в полости рта, наши зубы постоянно подвергаются воздействию этих бактерий, а не только во время еды. А «каждый раз во время еды», мы поставляем этим бактериям углеводы, то есть дополнительное сырье, необходимое им для вырабатывания кислоты, поэтому во время еды разрушительное действие бактерий усиливается [11].
Экспериментальная задачка №3. Зубная паста «Blend-a-med», содержащая фтористые соли, – одна из самых рекламируемых, для демонстрации её укрепляющих зубную эмаль свойств показывают впечатляющий опыт с куриным яйцом, которое после обработки этой зубной пастой не растворяется даже в уксусной кислоте. Проверьте экспериментально правдивость этой рекламы [11].
Как вы думаете, почему скорлупа половинки яйца, обработанной зубной пастой «Blend-a-med», не растворяется в уксусной кислоте? (КО: от растворения скорлупу яйца (карбонат кальция) защищает образовавшаяся на поверхности скорлупы пленка фторида кальция) Какими известными вам веществами можно защитить скорлупу яйца от «кислотного удара»? (интересные ответы: обмазать силикатным клеем, покрыть лаком для ногтей, окунуть половинку яйца в расплавленный парафин, натереть салом или мазутом).
Эвристическое задание 7. Установите последовательность слов и словосочетаний в логике: «причина – плохое следствие – «спаситель» – хорошее следствие – результат»
а) кислая среда, смородина, «Дирол», аскорбиновая кислота, нейтрализация, слюна (КО: 2,4, 1,3, 6, 5); б) «Лесной бальзам», pH=7, пирожное, молочная кислота, pH=3, углеводы (КО: 3, 6, 4, 5, 1, 2).
7. Блок «pH-графика» (КИП). Комментарий для учителя: Блок компьютерной интеллектуальной поддержки позволяет использовать для решения задач дополнительные возможности компьютерной среды, в том числе, приборы цифровой химической лаборатории, осуществление учащимися разных форм мыслительных операций на внутреннем плане способствует развитию абстрактного воображения. Комментарий для учащихся: Вам нужно пересесть за компьютерные столы. Первое задание: с помощью учителя ознакомиться с принципом работы цифрового pH-метра и провести контрольное измерение pH дистиллированной воды. Второе задание: осуществить несколько последовательных измерений значения pH раствора при протекании реакции нейтрализации сока лимона раствором «Lacalut»; сделать качественный анализ полученного графика: как изменяется «погода»-среда в исследуемом растворе в ходе реакции.
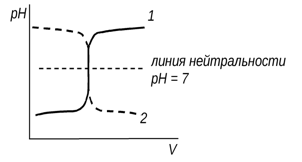
Рис. 10. Схематичный график изменения pH в реакции нейтрализации
сока лимона раствором «Lacalut»
8. Блок «Разноцветная эмоция». Комментарий для учителя: Это блок обратной связи, эмоциональной оценки занятия, ориентированный на развитие рефлексии учащихся по двум направлениям: оценка задач, которые надо было решать (интересно-не интересно) и оценка своих ресурсов: насколько успешно задачи были решены (справился-не справился). Комментарий для учащихся: Оцените своё эмоциональное состояние в ходе занятия: колба с пузырьками газа красного цвета – занятие понравилось, настроение отличное; колба с пузырьками газа синего цвета – занятие скучное, хорошо, что закончилось.

Рис. 11. «Маркеры» эмоционального состояния

Рис. 11. «Маркеры» эмоционального состояния
Не каждый ученик может стать «химическим» гением, но существует множество полезных и практических уровней, на которых можно с успехом применять креативные приёмы решения эвристических задач (и не только по химии). Полученные результаты свидетельствуют о том, что адаптированная методология НФТМ-ТРИЗ является «ключиком» к развитию творческого начала младших школьников и достаточно успешно в формате учебного предмета решает задачи развития способности учащихся оптимально использовать «то, что знаешь, так, как умеешь, и там, где находишься».
Ссылки на источники
1. Алексинский В. Н. Занимательные опыты по химии. Книга для учителя. – М.: Просвещение, 1995. – 96 с.
2. Ахмадулина Б. А. «Газированная вода», стихи [электронный ресурс] – Режим доступа. – URL: http://stroki.net/content/view/2259/13/ [дата обращения 30.11.2015]
3. Горев П. М., Утёмов В. В. Формула творчества: решаем открытые задачи. Материалы эвристической олимпиады «Совёнок»: учебно-методическое пособие. – Киров: Изд-во ВятГГУ, 2011. – 288 с.
4. Горев П. М., Утёмов В. В. Экспедиция в мир творчества: учебно-методическое пособие. – Киров: Изд-во «О-Краткое», 2013. – 128 с.
5. Горев П. М., Утёмов В. В. Полёт к горизонтам творчества: Учебное пособие. – Киров: Изд-во «О-Краткое», 2013. – 112 с.
6. Горев П. М., Утёмов В. В. Волшебные сны Совёнка: учебно-методическое пособие. – Киров: Изд-во ВятГГУ, 2012. – 144 с.
7. Загорский В.В. Воспитать ученого. // Образование: исследовано в мире. Международный научный педагогический интернет-журнал с библиотекой-депозитарием. – 2003. – [электронный ресурс] – Режим доступа. – URL: http://www.oim.ru. [дата обращения 30.11.2015]
8. Зиновкина М. М. Многоуровневое непрерывное креативное образование и школа. Пособие для учителей. – М.: Изд-во «Приоритет-МВ», 2002. – 48 с.
9. Оржековский П. А. и др. Творчество учащихся на практических занятиях по химии: Книга для учителя. – М.: Изд-во «АРКТИ», 1999. – 152 с.
10. Пашкевич С. В. Основы химии: программа развивающего курса для начальной школы. – Екатеринбург: ООО «Изд-во УМЦ УПИ», 2011 – 28 с.
11. Пичугина Г. В. Повторяем химию на примерах из повседневной жизни. Сборник заданий для старшеклассников и абитуриентов с ответами и решениями. М.: АРКТИ, 2000. – 136 с.
12. Утемов В. В, Зиновкина М. М., Горев П. М., Педагогика креативности: прикладной курс научного творчества: Учебное пособие. – Киров: АНОО «МЦИТО», 2013. – 212 с.
