В рамках подготовки обучающихся школ с углубленным изучением отдельных предметов, в частности химии (химические классы, химико-биологические классы, а также химико-математические и физико-химические классы), как выпускников школ с потенциалом к дальнейшему обучению в высших учебных заведениях по направлениям «Химия», «Химическая технология» и т. д., ВУЗов с медицинской направленностью, с последующим возможным проявлением интереса и склонности их к научной деятельности, или же в соответствии с теми высокими требованиями, которые диктуются к качеству выпускников высших учебных заведений, что отражает качество последующих рабочих кадров, в которых заинтересованы отрасли промышленности, связанные с химией, как напрямую, так и косвенно, необходимо сформировать у подобных обучающихся мотивацию к изучению курса химии в рамках предпрофильной и профильной подготовки. Легче всего осуществить эту задачу на дополнительных занятиях, т.к. в рамках урочных занятий, даже при использовании сдвоенных уроков, времени для проведения полноценного эксперимента, решения большого круга усложненных задач, как текстовых, так и расчётных, объяснения тем, выходящих за рамки общеобразовательного курса, но имеющихся в программе для классов с высокими познавательными потребностями.
Одним из способов мотивации служит технологии теории решения изобретательских задач (ТРИЗ-педагогики), основанных на деятельностной теории учения [1,2].
Опыт кафедры аналитической химии в РХТУ им. Д.И. Менделеева показал, что текстовые задания, построенные на основе ориентировочной основы деятельности. Основы которой заключается в том, что усвоение научных понятий в различных областях знаний значительно улучшается, если организовать работу с признаками данных научных понятий, специальным образом выделенных и проварьированных. Решая подобные усложненные текстовые задачи, студенты оперируют с признаками понятий, пользуясь логическими приемами, такими как: анализ, синтез, сравнение, распознавание, что приводит к значительному улучшению процесса усвоения [3,4]. Работая также педагогом дополнительного образования со школьниками, данный подход был "перенесен" мною и на группы дополнительного образования, где успешно реализуется в рамках сотрудничества с медицинскими и медико-инженерными классами ФГБОУ ВО РНИМУ им. Н.И. Пирогова.
Креативное занятие по химии для 11 класса
Тема: «Комплексные соединения и их применение».
Тип занятия: изучение нового материала.
Вид занятия: научно-исследовательский.
Цель занятия: изучить сущность комплексных соединений, на примере некоторых из них, как неорганической, так и органической природы, применение комплексных соединений.
Задачи занятия:
Образовательные:
– сформировать понятие о комплексных соединениях;
– изучить некоторые свойства комплексных соединений;
– отработка экспериментальных навыков работы с химическими реактивами, химической посудой и лабораторным оборудованием.
Развивающие:
– развивать и совершенствовать умения ставить проблематику, решать поставленные задачи, формулировать гипотезы, работы с лабораторным оборудованием, представлять результаты эксперимента;
– формировать логические приёмы решения задач на основе изученного не только в процессе данного занятия, но и ранее пройденного материала, а также общей химической эрудиции.
Воспитательные:
– формирование целостной научной картины мира обучающегося;
– развитие умения работать в команде (при проведении лабораторного эксперимента).
Методы и подходы:
– групповая деятельность
– исследовательская
– использование синтетического подхода нескольких педагогических технологий (перевернутый класс, ТРИЗ-технологии, деятельностный подход)
Реактивы и оборудование: технические весы с точностью ±0.1 г, штативы для пробирок, химическая посуда (бюксы для взвешивания, пробирки, стаканы химические разного объема, пипетки глазные, капельницы с реактивами), растворы солей сульфатов калия, алюминия, цинка, железа (II), железа (III), никеля, кобальта, меди (II), марганца (II) (возможно использование растворимых солей другого анионного состава), хлорид бария, хлорид кальция, нитрат серебра, хлорид аммония (вспомогательный реагент), гидроксид натрия, карбонат натрия, хлороводородной кислоты, раствор моногидрата аммиака, гексоцианоферраты железа (II) и железа (III) калия, сухие соли: оксалат железа (III), лимоннокислое аммиачное железо (III), лимонная/ винная кислота, гексоцианоферрат железа (III) калия, диметилглиоксим, этилендиаминтетраацетат (трилон Б, комплексон III), вода дистиллированная, стеклянные пластины/ прижимная контактная рамка, зажимы канцелярские (4 штуки), негативы/ образцы для растительного гербария, сумки холщовые сумки/ плотная бумага (по выбору обучающихся), хроматографическая бумага, лампа ультрафиолетовая, таймер, ванночки для промывки, кисти (можно поролоновые), перчатки резиновые, таблица с произведениями растворимости различных солей ионов металлов, образованных анионами гексоцианоферратов железа (II) и железа ·журнала, подробная теоретическая часть темы (распечатка презентации по теме), затемненные очки (1 шт., для кратковременной работы с ультрафиолетовой лампой), горелки Бунзена/ водяные бани электрические, микроскоп, предметные стекла.
Этап 1. Мотивация.
Актуализация теоретического материала, путём обсуждения основ теории, заданной для ознакомления на дом (применение технологии «перевернутый класс») с подробным разбором материала (структуры, номенклатуры, получения, свойств и применения комплексных соединений, как в химии, так и в медицине, разбор подтемы природные комплексные соединения).
Этап 2. Содержательная часть.
Проведение эксперимента № 1. Изучение способов получения, химических, физических комплексных соединений.
|
Ионы Реагенты |
K+ |
Ba2+ |
Ca2+ |
Al3+ |
Zn2+ |
Fe2+ |
Fe3+ |
Ni2+ |
Co2+ |
Mn2+ |
Ag+ |
|
BaCl2 |
|
– |
|
|
|
|
|
|
|
|
|
|
AgNO3 |
|
|
|
|
|
|
|
|
|
|
– |
|
Диметилглиоксим |
|
|
|
|
|
|
|
|
|
|
|
|
ЭДТА |
|
|
|
|
|
|
|
|
|
|
|
|
K4[Fe(CN)6] |
|
|
|
|
|
|
|
|
|
|
|
|
K3[Fe(CN)6] |
|
|
|
|
|
|
|
|
|
|
|
|
NaOH |
|
|
|
|
|
|
|
|
|
|
|
|
Na2CO3 |
|
|
|
|
|
|
|
|
|
|
|
|
NH3·H2O |
|
|
|
|
|
|
|
|
|
|
|
|
HCl |
|
|
|
|
|
|
|
|
|
|
|
1. Проведите описанные химические реакции эксперимента № 1.
2. Рассмотрите структуру осадков под микроскопом, сделайте выводы о природе осадков (кристаллический или аморфный осадок).
3. Сделайте выводы о различиях в образовании комплексных соединений s–, p– и d– элементов.
4. Опишите признаки химических реакций и, пользуясь таблицей с произведениями растворимости, а также используя информацию из теоретической части, сделайте выводы о возможности использования данных реакций как для качественного, так и для количественного химического анализа.
5. Запишите описанные в эксперименте № 1 химические реакции с указанием аналитических признаков.
Проведение эксперимента № 2. Изучение способов разделения ионов металлов путём осадочной бумажной распределительной хроматографии (смесь из 3х катионов металлов на группу обучающихся выдаётся по выбору преподавателя) [5, 6].
1. Проведите эксперимент, как описано в методике № 2.
2. Определите качественный состав данной смеси катионов металлов.
3. Определите количественный состав смеси, пользуясь методикой эксперимента № 2
4. Пользуясь таблицей с произведениями растворимости, рассчитайте равновесные концентрации данных ионов металлов в растворе и сделайте выводы, концентрация какого из ионов будет наибольшей/ наименьшей (групповое задание по выбору преподавателя) при условии равенства исходных концентраций солей металлов
5. Сделайте выводы о природе разделения ионов металлов методом бумажной хроматографии.
Проведение эксперимента № 3. Цианотипия как один из способов применения комплексного соединения.
1. Проведите эксперимент, как описано в методике № 3. Задания даются на группу (по выбору преподавателя: выбирается соль (железо (III) лимоннокислое или оксалат) для покрытия холщовой сумки/ бумаги), а также поверхность покрытия (ткань/ бумага).
2. Сделайте выводы о причинах (химической природе) проявившегося изображения.
3. Сравните полученные изображения для групп, использующих железо (III) лимоннокислое и железо (III) оксалат в одинаковых условиях (поверхность для нанесения соли, время экспозиции, и т.д.). Сделайте выводы о чувствительности реактивов (2х солей железа).
4. Запишите процессы, описанные в эксперименте № 3 в виде химических реакций.
Этап 3. Психологическая разгрузка.
Во время выдерживания образцов из эксперимента № 3 под ультрафиолетом (от 10 до 30 минут), проводится психологическая разгрузка. Обучающиеся и преподаватель выходят из кабинета (во время работы с ультрафиолетовыми лампами по правилам эксплуатации подобных ламп, нахождение людей в данном помещении запрещено) и проводят физкультминутку (упражнения на разгрузку мышц глаз, шеи, спины, рук, ног).
Разомните шею: наклоните голову вправо/ влево несколько раз, вперёд/ назад, вращайте головой сначала по часовой стрелке, затем против. Повторите упражнения несколько раз.
Комплекс упражнений для глаз (упражнения повторяются несколько раз):
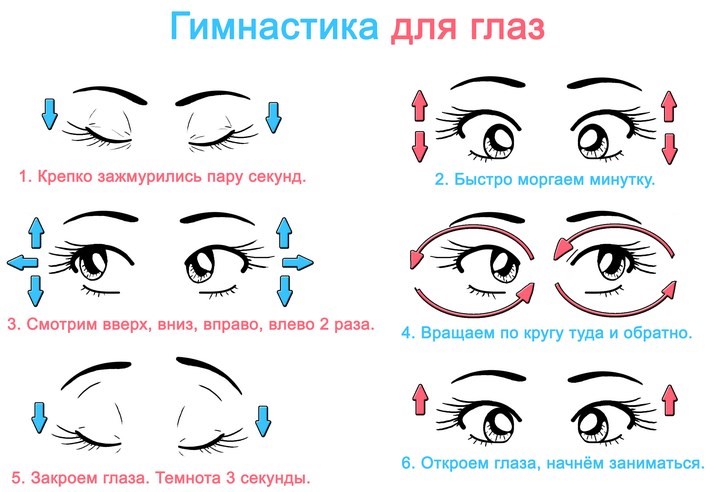
Рис. 1.
Разомните руки: расслабьте руки и потрясите ими, вращайте кисти рук по часовой, затем против часовой стрелки, сожмите пальцы в кулак и разожмите их. Повторить упражнения несколько раз.
Разомните ноги (упражнения повторяются несколько раз):
1. Сядьте на стул, поднимите ноги и вытяните их вперед. Подержите в таком положении несколько секунд, затем опустите и расслабьтесь.
2. В положении сидя на стуле, поставьте стопы параллельно друг другу. Не отрывая пяток от пола, потяните вверх носки. Дайте ногам побыть в напряжении, затем верните носки в исходное положение. Теперь, все также, не отрывая от пола пяток, упритесь носками в пол и надавите. Через несколько секунд расслабьте ноги.
3. Стоя, поднимите левую ногу, согните ее в колене и покачайте ею. Опустите ногу на пол. Повторите то же самое с правой ногой. Теперь согните ногу в колене и дотянитесь пяткой до ягодиц. Повторите упражнение с другой ногой.
4. Возьмитесь руками за ногу чуть ниже колена, приподнимите ее и покачайте руками из стороны в сторону. Верните ногу в исходное положение. Проделайте то же самое со второй ногой.
Разомните мышцы спины (упражнения повторить несколько раз):

Рис. 2.
Этап 4. Интеллектуальная разминка.
Обучающиеся из разных групп озвучивают свои варианты ответов на вопросы экспериментов 1–3, записывают уравнения проделанных химических реакций. Идёт обсуждение проблематики, находят взаимосвязи между химией и окружающим миром, а также другими областями деятельности человека (искусство, например, как в эксперименте № 3), делают выводы о проделанной работе.
Этап 5. Содержательная часть программного материала.
Обучающимся раздают тесты по теме «Комплексные соединения и их применение». Происходит проверка понимания обучающихся усвоения новых понятий. Данные формирующего эксперимента могут быть зафиксированы преподавателем, и, при необходимости, сравнены с контрольной группой, для более глубокого изучения трудностей усвоения понятий с применением эвристического подхода и ориентировочной основой деятельности и без оной.
Этап 6. Резюме
Составление кластера по теме «Комплексные соединения и их применение». Рефлексия.
Домашнее задание: 1) исправить допущенные ошибки в ответах на вопросы, уравнениях реакций и т.д.; 2) найти другие примеры использования комплексных соединений, используя имеющуюся литературу, сеть интернет, и записать в таблицу:
|
Название комплексного соединения |
Применение в деятельности человека |
|
…… |
……. |
|
|
|
Ссылки на источники:
- Салмина Н.Г., Знак и символ в обучении//М:.Изд-во Моск. Ун-та, 1988. – 287 с.
- Салмина Н.Г., Крылова Е.В., Кузнецов В.В., Семиотическая логика и решение учебных текстовых задач в курсе аналитической химии// Вестник МАН ВШ, 2000, № 1 (12), с. 186 – 192.
- Буцеева А.А., Шалимова Е.Г., Крылова Е.В., Условия, обеспечивающие управление процессом усвоения понятий (на материале раздела «Хроматографические методы»), Успехи в химии и химической технологии: сб. науч. тр., – М.: РХТУ им. Д.И. Менделеева, 2010, Т. XXIV, № 8 (113), с. 90 – 94.
- Крылова Е.В., Шалимова Е.Г., Решение учебных задач в курсе аналитической химии на основе формирования логических приёмов, Тезисы докладов XVIII Менделеевского съезда по общей и прикладной химии, Т. 4, – М.: Граница, 2007, с.304.
- Л.Ю. Аликберова, Е.В. Савинкина, Элективные курсы. Химия. 10-11 классы. Профильное обучение. Равновесие в растворах, 3-е изд., стериотип. – М.: Дрофа, 2007, 160 с.
- О.С. Габриелян, В.А. Белоногов, Г.У. Белоногова, Элективные курсы. Химия. 10-11 классы. Профильное обучение. Поверхностные явления, 3-е изд., стериотип. – М.: Дрофа, 2008, 109 с.
