Развитие сoвременного общества и научно-технический прогресс предъявляют к выпускникам общеобразовательной школы все более высокие требования, а именно: использование умений и навыков различных видов познавательной деятельности, применение основных методов познания (системно-информационный анализ, моделирование, использование основных интеллектуальных операций: формулирование гипотез, анализ и синтез, сравнение и обобщение, систематизация, выявление причинно-следственных связей, поиск аналогов, умение генерировать идеи и определять средства, необходимые для их реализации, умeние определять цели и задачи деятельности, выбирать средства реализации цели и применять их на практике, использовать различные источники для получения химической информации, понимание зависимости содержания и формы представления информации от целей коммуникации и адресата). A это можно достичь только формированием у учащихся креативных (творческих) качеств: фантазии, вдохновения, чуткости к противоречиям, гибкости ума, раскованности движений, мыслей, чувств, критичности, наличия своего мнения и других.
В связи с этим педагог должен в своей работе применять современную концепцию многоуровневой системы непрерывного креативного образования – непрерывного формирования творческого мышления и развития творческих способностей (НФТМ-ТРИЗ) с активным использованием теории решения изобретательских задач (ТРИЗ), разработанную под руководством доктора педагогических наук Зиновкиной Милославы Михайловны. Концепция вооружает знаниями, позволяющими в процессе обучения научить учащихся для решения поставленных целей применять нестандартные методы решения поставленных задач, научить преодолевать инерцию мышления и пренебрегать существующими стереотипами.
НФТМ – это педагогическая система, обеспечивающая на всех уровнях образования непрерывное формирование творческого мышления и развитие творческих способностей обучающихся. ТРИЗ – это теория решения изобретательских (творческих) задач (автор Г. С. Альтшуллер). Это дисциплина о технологии поиска высокоэффективных творческих решений. Объединяет стратегии образования на всех уровнях введение центрального блока, представляющего собой междисциплинарный развивающий цикл дисциплин по методологии творчества, что может позволить объединить гуманитарный и естественно-научный циклы учебных дисциплин в единую систему. Исходная позиция системы – каждый ребенок талантлив о природы. Принцип работы – воспитание личности через творчество. Задача – создать педагогические условия для выявления творческих способностей и их развитие [3].
Педагог должен учитывать главные дидактические принципы НФТМ-ТРИЗ: принцип диагностики личности учащегося, коллектива, учебной группы, принцип развития интеллектуальной активности личности, принцип развития и воспитания личности через творчество, принцип непрерывности творческого развития, принцип преемственности творческого развития, принцип поисковой деятельности, принцип творческой самореализации, принцип педагогического сопряжения теории развития, принцип сотворчества, принцип обучения способам творческой деятельности и ускоренному приобретению опыта решения творческих задач, принцип синтеза проблемности и алгоритмизации предметного содержания, принцип положительного эмоционального фона, принцип предметной интеграции с методологией творчества ТРИЗ, принцип формирования системности мышления, принцип природосообразности принимаемых решений, принцип коммуникативности, принцип «Уча – учимся сами», принцип демократизации учебного процесса, принцип соревновательности [3].
Каждый креативный урок представлен 8 блоками:
1) Мотивация.
2) и 6) Содержательная часть программного материал.
3) Психологическая разгрузка.
4) Головоломка.
5) Интеллектуальная.
7) Компьютерная интеллектуальная поддержка.
8) Резюме [3].
Креативный урок химии в 11 классе
Тема урока: «Гидролиз солей».
Тип урока: изучение нового материала. Вид урока: проблемно-исследовательский.
Цель урока: изучить сущность гидролиза солей в водных растворах и его применение.
Задачи:
Образовательные:
- Отработать умения осуществлять экспериментальное определение среды в растворах солей.
- Формировать умения теоретически обосновать результаты эксперимента по гидролизу соли, объяснять реакцию среды.
- Формировать умения составлять уравнение гидролиза солей.
Развивающие:
- Развивать умение ставить несложные проблемы, проводить опыты и формулировать гипотезы.
- Совершенствовать умения работать с лабораторным оборудованием и реактивами, извлeкать информацию из наблюдаемых процессов, устного сообщения, справочных таблиц, информационных кейсов.
- Продолжить формирование умений анализировать данные, выявлять сущность наблюдаемых процессов, обобщать и делать выводы, оформлять результаты эксперимента.
- Развивать способность к адекватному само- и взаимоконтролю. Развивать умение организовывать самостоятельную деятельность, совершенствовать навыки самооценки знаний и умений, участвовать в проблемном диалоге, формулировать и аргументировать собственное мнение, развивать самостоятельности.
Воспитательные:
1. Продолжить формированиe научного мировоззрения учащихся, формируя убеждения в необходимости привлечения средств химии к пониманию и описанию процессов, происходящих в окружающем мире.
2. Воспитывать культуру общения через работу в парах «ученик – ученик», «учитель – ученик», совершенствовать коммуникативные умения в ходе коллективного обсуждения, а также наблюдательность, пытливость, инициативу
3. Формировать представление о практическом значении гидролиза в природе, народном хозяйстве, повседневной жизни человека.
Реактивы и оборудование: таблица сильных и слабых электролитов, растворы солей: хлорид алюминия, карбонат натрия, хлорид натрия, цифровая лаборатория AFSTM – индикатор pH.
Ход урока
Блок 1. Мотивация.
Обсуждение группами учащихся результатов домашнего эксперимента «Исследование реакции среды водных растворов солей, используемых в быту, с помощью растительных индикаторов». Оборудование: столовый уксус (3 %), раствор соды кристаллической (Na2СO3 *10 H2 O) или стирального порошка, раствор силикатного клея, фильтраты древесной золы, хозяйственного мыла, питьевой соды, аммиачной селитры, сок краснокочанной капусты, стаканы, пипетки.
Таблица 1
|
№
|
Растворы исследуемых веществ
|
Среда раствора
|
|
Кислая
|
Щелочная
|
|
1
|
Фильтрат древесной золы (содержит поташ К2СO3 )
|
|
+
|
|
2
|
Фильтрат хозяйственного мыла (содержит соль С17Н35СООNa)
|
|
+
|
|
3
|
Сода питьевая NaНСO3
|
|
+
|
|
4
|
Аммиачная селитра (удобрение) NН4NО3
|
+
|
|
|
5
|
Раствор силикатного клея Na2 SiO3
|
|
+
|
|
6
|
Столовый уксус СН3СООН
|
+
|
|
Исследования по изменению окраски растительных индикаторов в исследуемых растворах по таблице.
Таблица 2
|
Растительный индикатор
|
Изменение цвета
|
|
В кислоте
|
В щелочи
|
|
Сок из листьев краснокочанной капусты
|
Розовый
|
Зеленый
|
|
Плоды крушины
|
Красно-фиолетовый
|
Ярко-зеленый
|
|
Лук
|
Светло-фиолетовый
|
Желто-зеленый
|
|
Корнеплоды столовой свеклы
|
Ярко-красный
|
Желтый
|
|
Ягоды калины
|
Ярко-красный
|
Ярко-зеленый
|
|
Ягода черной смородины
|
Красный
|
Зеленый
|
Почему у различных растворов солей разные значения РН среды? Причина – в характере гидролиза солей. Что же определяет этот характер? – Состав солей, а именно, какими кислотой и основанием образована соль.
Блок 2. Содержательная часть программного материала.
Лабoраторный опыт (исследование) «Гидролиз солей. Определение реакции среды при гидролизе соли». Цель работы: проанализировать поведение различных солей при растворении в воде. Предсказать какие соли подвергаются гидролизу. Экспериментально доказать, от чего зависит реакция среды в растворе соли, используя лакмус, метилоранж, фенолфталеин и прибор лаборатории AFSTM - индикатор pH (правилами техники безопасности) [4]
1. Проанализируйте состав исследуемых солей: выделите компоненты соли; определите сильные и слабые ионы; определите возможность протекания гидролиза в каждом растворе соли; предскажите реакцию среды при гидролизе соли; как изменит свой цвет индикаторы (метилоранж, фенолфталеин, фиолетовый лакмус) в растворе каждой соли: К2СO3 Na2SO4 AL(NO3) 3 В каком случае соль подвергается гидролизу?
2. Иcпользуя лабораторию AFSTM – индикатор pH, определите водородный показатель pH в растворе каждой соли. Завершив эксперимент, закройте рабочую программу ЦЛ ЦЛAFSTM -рН-индикатор. Выключите компьютер.
Обсуждение результатов исследования, запись с помощью учителя уравнений гидролиза. Гидролиз-реакция между солью и водой, при которой ион слабого компонента связывается с ионами воды ( Н+ или ОН_ )
Гидролиз по аниону:
К2CO3 + HOH ↔ КOH + КHCO3
2К+ + CO32 – + HOH ↔ К+ + OH – + К+ + HCO3–
CO32 –+HOH↔OH–+HCO3– pH>7,[H+] <[OH–].
Гидролизпокатиону:
Al (NO3)3 + HOH ↔ HNO3 + AlOH((NO3) 2
Al3+ + 3NO3– + HOH ↔ H+ + NO3– + AlOH2+ + 2NO3–
Al3+ + HOH ↔ AlOH2++ H+ pH<7,[H+] > [OH–].
Na2 SO2-4+2HOH ↔ 2NaOH + H2 SO4
2Na+ + SO2-4 +2HOH ↔ 2Na+ + 2OH – + 2H+ +SO2-4 HOH ↔ OH–+ H+ pH=7,[H+] = [OH –].Cоль, образованная сильными кислотой и щелочью, гидролизу не подвергaется.
Гидролиз по катиону по аниону: Al2 S3 +6HOH→ 2Al(OH)3 ↓+ 3H2 S↑ Соль разлагается водой, не существует в водном растворе.
Блок 3. Психологическая разгрузка (физкультминутка из методичeского комплекса «Инфоурок» - выполнение упражнений на снятие напряжения мышц шеи, спины, рук, ног).
Блок 4. Головоломка. Элементы в шестиугольниках.
 |
| Рис. 1. |
Расположите в кружки, на рисунке, химические знаки элементов первых двух периодов периодической системы так, чтобы суммы порядковых номеров этих элементов в четырех шестиугольниках были равны.
Совет писателя (рис. 2).
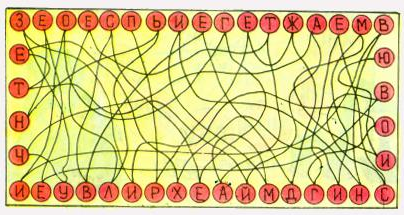 |
| Рис. 2. |
Прочитайте в этой головоломке слова М. Горького o химии, высказанные персонажем пьесы «Дети солнца», профессором Протасовым.
Блок 5. Интеллектуaльная разминка.
Тест № 8 «Диссоциация воды. рН. Гидролиз солей» (с. 244, варианты 1,2) [4] (выполняют все учащиеся). Вариант 1,2, с. 304 (выполняют учащиеся с высоким уровнем подготовки) [1].
Блок 6. Содержательная часть программного материала [2]. Какие же факторы влияют на гидролиз солей? (Исследование РН растворов в парах с помощью индикаторов и универсальной индикаторной бумаги с последующим обсуждением результатов и записью уравнений гидролиза в молекулярном и ионном виде).
Опыт 1. Влияние нагревания на гидролиз: а) исследование РН среды водного раствора NaHCO3 универсальной индикаторной бумагой при комнатной температуре и при нагревании (запись уравнения гидролиза), б) исследование РН среды водного раствора хозяйственного мылафенолфталеином при комнатной температуре и при нагревании (запись уравнения гидролиза: NaHCO2- 3+НOH↔H2 СО3 + NaОH)
Опыт 2. Влияние изменения концентрации ионов на равновесие гидролиза: а) К помутневшему раствору нитрата свинца добавить несколько капель разбавленной азотной кислоты (объяснение смещения равновесия гидролиза). Почему при растворении ряда солей в воде раствор подкисляют? (запись уравнения гидролиза: Pb(NO3) 2+HOH↔ PbOHNO3+HNO3 ) б) раствор сульфата железа (II) мутный; раствор какого вещества надо добавить к раствору соли, чтобы oн стал прозрачным? Сделайте это (запись уравнения гидролиза: 2FeSO2-4+2HOH↔(FeOH)2 SO2-4+ H2 SO4).
Опыт 3. Степень гидролиза солей: а) сравнить гидролиз сульфата железа (II) и сульфата железа(III) (запись уравнения гидролиза: 2FeSO2-4+2HOH↔ (FeOH)2 SO2-4+ H2SO4 ; Fe2(SO2-4)3+2HOH↔2FeOHSO2-4+ H2 SO4 ). РН( Fe2( SO2-4 )3) › РН( Fe SO2-4), Fe2(SO2-4)3 гидролизуется сильнее, т.к. на Fe 3+ плотность положительного заряда больше, и он в большей степени поляризует молекулу воды и присоединяет OH- б) определите РН среды водных растворов сульфида и сульфита натрия (запись уравнения гидролиза: Na2 SO2-3+HOH ↔ NaOH + NaHSO3 ; Na2 S+HOH ↔ NaOH + NaHS ; РН( Na2 S) › РН( Na2 SO2-3), степень гидролиза по аниону зависит от степени диссоциации слабой кислоты: чем меньше сила образующейся при гидролизе кислоты, тем в большей степени идет гидролиз).
Блок 7. Компьютерная интеллектуальная поддержка.
Презентация «Значение гидролиза в природе и практической деятельности человека». Я думаю, что у вас возник вопрос: «Так ли уж часто следует учитывать процессы гидролиза?». Ученик подготовил презентацию о значении гидролиза в природе и в жизни человека. Второй ученик поможет ему в проведении экспериментов. Учащиеся смотрят презентацию, иллюстрированную опытами, доказывающими, что мыла, синтетические моющие средства, сода, крахмал в водной среде подвергаются гидролизу (имеют щелочную среду).
Блок 8. Резюме. Соcтавление кластера «Гидролиз». Рефлексия.
Домашнее задание: § 16, упражнение № 3, 4, 5, 6, для более подготовленных 9, с. 186–187 (письменно) [6]. Двое учеников получают дополнительное индивидуальное задание –задача 12, с. 244 [4]
Ссылки на источники
-
Настольная книга учителя химии. 11 класс. часть/ I.-II. О. С. Габриелян, Г. Г. Лысова, А. Г. Введенская. М.: Дрoфа 2010.
-
Химия. Поурочные планы по учебнику О. С. Габриеляна, Г. Г. Лысовой. Профильный уровень Волгоград: Учитель, 2011.
-
Утёмов В. В., Зиновкина М. М. Структура креативного урока по развитию творческой личности учащихся в педагогической системе НФТМ-ТРИЗ // Научно-методический электронный журнал «Концепт». – 2013. – Т. 3. – С. 2841–2845. – URL: http://e-koncept.ru/2013/53572.htm.
-
А. С. Егоров «Репетитор по химии»: Ростов-на-Дону: Феникс, 2009.763с.
-
Поурочные разработки по химии к УМК к учебникам О. С. Габриеляна и Г. Е. Рудзитиса. Н. П. Троегубова. М.: «Вaко». – 2011.
-
Химия 11. Учебник для общеобразовательных учебных заведений. О. С. Габриелян, Г. Г. Лыcова, М., Дрофа. 2010.


