Девиз: Если то, о чем тебе известно, ты один иль сотни слышишь раз,
Не ропщи: «Мол мне - не интересно». Повторенье образует нас!
Цели:
образовательная: закрепить и систематизировать полученные на уроках знания о классах неорганических веществ;
развивающая: развивать логическое мышление на примерах генетической связи между классами неорганических веществ и при решении экспериментальных задач;
воспитательная: воспитывать чувство коллективизма, ответственности, взаимопомощи, взаимоподдержки и взаимоуважения в условиях работы в командах.
Задачи для учащихся:
1. Знать определения важнейших классов неорганических соединений.
2. Уметь составлять формулы и давать названия неорганическим соединениям.
3. Уметь записывать химические свойства неорганических веществ.
4. Вырабатывать практические навыки при решении экспериментальных задач.
Оборудование: SMART boаrd, карточки с заданиями, карточки для самостоятельной работы, кроссворды (3 шт.), 3 штатива с реактивами: HCl, NaOH, H2O, Na2SO4, индикаторы – фенолфталеин, лакмус, метилоранж.
Тип урока: обобщение и закрепление знаний.
Форма проведения урока: в виде игры «Клуб находчивых химиков».
ХОД урока
О проведении игры – «Клуба находчивых химиков» (КНХ) объявляется заранее, дается домашнее задание:
1) придумать название команды, выбрать капитана;
2) подготовить сообщения о применении неорганических веществ в быту, в медицине, в сельском хозяйстве.
В игре принимают участие 3 команды.
I. Организационная часть.
1) Организационный момент
2) Подготовка учащихся к проведению игры КНХ.
Учитель: «Сегодня мы собрались в клубе находчивых химиков для того, чтобы обобщить полученные вами знания об оксидах, кислотах, основаниях, солях и получить новые. На этом уроке вы вспомните о химических свойствах важнейших классов неорганических соединений и взаимосвязи между ними.
Для того, чтобы ваши знания были правильно оценены, у нас на уроке присутствует жюри - учащиеся 10-х классов: Ковригина Арина, Иноземцева Анастасия, Платонова Анна и родители: Сударева Е.М., Рудниченко О.В.»
II. Основная часть урока.
Наша игра пойдет по следующим этапам:
- Приветствие команд.
- Разминка.
- Конкурс капитанов.
- Конкурс эрудитов.
- Проверь себя.
- Это интересно знать
Итак, начинаем нашу игру КНХ (команды рассаживаются по группам).
1) ПРИВЕТСТВИЕ
(отводится по одной минуте на приветствие, оценивается в 3 балла)
1 команда – «КИСЛОТЫ».
2 команда – «ВОДОРОД».
3 команда – «ОСНОВАНИЯ».
2) РАЗМИНКА
1. (Правильный ответ – 1 балл.) Ведущий поочередно каждой команде задает вопросы:
1) Какие вещества называются основаниями?
2) Какие вещества называются кислотами?
3) Какие вещества называются солями?
2. Задание выполняется с использованием интерактивной доски.
(Правильный ответ – 3 балла.)
К доске выходят по одному представителю от каждой команды и при помощи цветных фломастеров подчеркивают формулы соединений, согласно своему заданию.
На интерактивной доске вы видите формулы неорганических веществ: Ca, H2SO4, KCl, NaOH, KNO3, SO3, MgCO3, KOH, Cl2, Cu(OH)2, HNO3, Fe(OH)3, HCl, Ca(HSO4)2, H3PO4, NH3.
Выберите из них:
1 команда – соли (красный цвет)
2 команда – основания (жёлтый цвет)
3 команда – кислоты (синий цвет)
3. Задание оценивается в 6 баллов (5 баллов за уравнения и 1 балл за быстроту решения; это очко присуждается команде, которая быстрее, а главное, правильно записала все возможные уравнения реакций).
С какими из перечисленных веществ будут реагировать данные вещества?
Командам раздаются карточки с заданиями, которые выполняются на отдельных листах. Каждый участник команды пишет по одному уравнению реакции.
1) HCl: Zn, AgNO3, Cu, S, CaO, ZnCl2, Cu(OH)2, Na2CO3.
2) CuCl2: HNO3, KOH, Fe, K2CO3, HCl, AgNO3, Cu, H3PO4.
3) NaOH: H2SO4, CuCl2, CO2, Cl2, HNO3, KOH, CaO,
4. (Правильный ответ – 3 балла.)
Задание выполняется с использованием интерактивной доски.
Из приведенного перечня CO2, CaSO4, H2SO4, S, Ca(OH)2, Na, SO2, CaO, NaOH, SO3, BaSO4, Ca, Na2O, AlCl3, MgO, Na2SO4 выберите формулы тех веществ, которые составляют генетический ряд:
1) для команды «КИСЛОТЫ» - генетический ряд кальция;
2) для команды «ВОДОРОД» - генетический ряд серы;
3) для команды «ОСНОВАНИЯ» - генетический ряд натрия.
По одному представителю от каждой команды выходят к доске и составляют заданный генетический ряд. Из ряда приведенных формул выносят нужные и составляют ряд.
Затем ведущий на интерактивной доске открывает затененную часть экрана для проверки составленных цепочек.
1) Ca → CaO → Ca (OH)2 → CaSO4
2) S → SO2 → SO3 → H2SO4
3) Na → Na2O → NaOH → Na2SO4
5. (Правильный ответ – 3 балла.)
Задание выполняется с использованием интерактивной доски.
Установите соответствие между оксидами и соответствующими гидроксидами.
В один столбик записаны формулы оксидов, во второй – формулы гидроксидов (в виде кислот и оснований). Представители от команд фломастерами при помощи стрелок устанавливают данные соответствия.
Команда «КИСЛОТЫ» Команда «ВОДОРОД» Команда «ОСНОВАНИЯ»
Оксиды Гидроксиды Оксиды Гидроксиды Оксиды Гидроксиды
SO2 H2SO4 Al2O3 H2SO3 B2O3 HNO3
Cl2O7 HCl P2O5 H2CO3 K2O H3BO3
CaO H2SO3 CO2 H3PO4 N2O5 HNO2
Ca(OH)2 Al(OH)3 KOH
HClO4 H2SiO3 H2CrO4
3) КОНКУРС КАПИТАНОВ
1. (Задание оценивается по пятибальной шкале).
Перед вами на экране расположена таблица. Используя ее данные, каждый из капитанов за 1 минуту должен составить формулы разных солей, комбинируя нижеприведенные составные части солей по горизонтали (слева направо) и вертикали (сверху вниз) при условии, что солеобразующие части стоят рядом. Назовите полученные соли (формулы не должны повторяться).
Побеждает тот капитан, кто составит больше правильных формул за отведенный промежуток времени. Индексы в формулах капитаны расставляют самостоятельно.
|
Zn
|
|
K
|
S
|
O
|
|
Ba
|
С
|
O
|
S
|
Na
|
|
Ca
|
Р
|
O
|
Zn
|
K
|
S
|
Cu
|
|
Mg
|
S
|
O
|
K
|
H
|
S
|
O
|
N
|
О
|
| |
|
|
|
|
|
|
|
|
2. (Оценивается в 3 балла)
Задание выполняется на интерактивной доске.
Выявите в каждом ряду закономерность, в соответствии с которой заполнены клетки формулами разных неорганических веществ. И в соответствии с правилом, вставьте в пустые клетки подходящие формулы.
Капитаны команд при помощи фломастеров вписывают в таблицы необходимые формулы (таблицы заготавливаются заранее). По окончанию ведущий приоткрывает затененную часть экрана для проверки.
На интерактивной доске таблицы:
1)
2)
3)
4) КОНКУРС ЭРУДИТОВ
1. Каждой команде задаются вопросы. На обдумывание ответа дается 30 секунд. Каждый правильный ответ оценивается в 3 балла.
1) Какой великий русский химик был поэтом, физиком, географом, геологом, стекловаром? (М.Ю.Ломоносов)
2) Какая кислота всегда находится в желудках здоровых людей, а при недостатке этой кислоты ее употребляют как лекарство? (соляная кислота)
3) Какой камень искали химики средневековья, хотя такого камня в природе не было и нет? («философский»)
2. Кроссворд. Решение кроссворда оценивается в 5 баллов.
Каждой команде на столы раздаётся кроссворд, который после выполнения сдается жюри для оценивания.
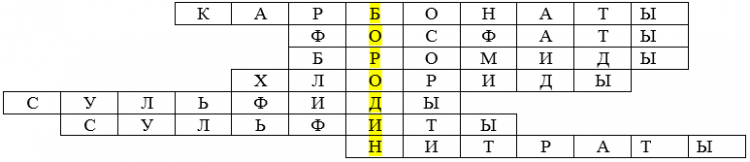
Надо заполнить клетки по горизонтали так, чтобы по вертикали «А» можно было прочитать фамилию известного композитора – химика.
«А»
- Соли угольной кислоты.
- Соли фосфорной кислоты.
- Соли бромоводородной кислоты.
- Соли соляной кислоты
- Соли сероводородной кислоты
- Соли сернистой кислоты.
- Соли азотной кислоты.
(А. Бородин).
3. Экспериментальные задачи.
Ведущий раздает каждой команде карточки с задачами и штатив с необходимыми реактивами. Результаты опытов проверяют члены жюри и учитель. Задание оценивается в 5 баллов, при этом учитывается фактор скорости выполнения.
1) Задача для команды «КИСЛОТЫ».
В трех склянках без этикеток находятся прозрачные растворы гидроксида натрия, соляной кислоты и дистиллированной воды. Установите опытным путем, используя выданные вам реактивы, в какой склянке какой раствор.
2) Задача для команды « ВОДОРОД».
Даны три пробирки без этикеток с растворами щелочи, кислоты, дистиллированной воды. Определите, где какой раствор, используя только один индикатор (какой?).
3) Задача для команды «ОСНОВАНИЯ».
В трех пробирках находятся гидроксид натрия, соляная кислота, сульфат натрия. Определите содержание каждой пробирки, используя не более двух реактивов.
5) ПРОВЕРЬ СЕБЯ
Дифференцированное задание: ведущий предлагает цветные карточки с заданием «Осуществите превращения». красные – на оценку «5»
синие – на оценку «4»
зеленые – на оценку«3»
Ученик сам выбирает цвет карточки. На выполнение задания дается 5 минут. Оценки за это задание выставит учитель на следующем уроке.
Осуществите превращения:
На оценку «5»
1 вариант 2 вариант
KCl ← K → K2O → K2CO3 NaOH ← Na → Na2O → NaOH → NaH2PO4
↓ ↓
KOH → KH2PO4 NaCl
На оценку «4»
1 вариант 2 вариант
CuCl2 → Cu(OH)2 → CuO → Cu(NO3)2 Ca → CaO → Ca(OH)2
↓ ↓
Cu CaSO4 → Ca(OH)2
На оценку «3»
1 вариант 2 вариант
K → K2О → KOH → K3PO4 Р → Р2О5 → Н3РО4 → К3РО4
6) ЭТО ИНТЕРЕСНО ЗНАТЬ
От каждой команды выступает ученик с заранее приготовленным сообщением на тему: «Применение неорганических веществ:
1 команда – в быту, 2 команда - в медицине, 3 команда - в сельском хозяйстве»
Каждое сообщение оценивается в 3 балла.
III. Заключительная часть.
Жюри подводит итоги и объявляет победителей среди команд и среди капитанов.
IV. Домашнее задание:
1).Подготовиться к практической работе: стр.114 пр.раб.№6, задачи 1, 3, 5
2). Сделать слайдовую презентацию по основным классам неорганических веществ по плану: определение, классификация, физические и химические свойства, применение. (§ 14, 15, 16, 17, 18)
1 команда «КИСЛОТЫ» - для кислот
2 команда « ВОДОРОД» - для солей
3 команда «ОСНОВАНИЯ» - для оснований.
Примечание: динамичность урока дает возможность не проводить физкультминутку, перемещение по классу позволяет размять мышцы.
Таблица для подсчета баллов
|
Команда
«КИСЛОТЫ»
|
Команда
«ВОДОРОД»
|
Команда «ОСНОВАНИЯ»
|
|
I. Приветствие. (max 3 балла)
[-название команды; -эмблема; -эстетика оформления; -культура представления]
|
|
|
|
|
|
II. Разминка.
[-общая эрудиция команды; -точность ответа; -скорость ответа; -активность команды]
|
|
Задания-баллы Оценка
1зад – 1 балл _____
2 зад – 3балла _____
3 зад – 6 баллов _____
4 зад – 3 балла _____
5 зад –3 балла _____
|
Задания-баллы Оценка
1зад – 1балл _____
2 зад – 3балла _____
3 зад – 6 балов _____
4 зад – 3балла _____
5 зад – 3балла _____
|
Задания-баллы Оценка
1зад – 1балл _____
2 зад – 3балла _____
3 зад – 6 баллов _____
4 зад – 3 балла _____
5 зад –3 балла _____
|
|
III. Конкурс капитанов.
[ -точность ответа; -скорость ответа]
|
|
Задания-баллы Оценка
1зад – 5 баллов _____
2 зад – 3балла _____
|
Задания-баллы Оценка
1зад – 5баллов _____
2 зад – 3 балла _____
|
Задания-баллы Оценка
1зад – 5 баллов _____
2зад – 3 балла _____
|
|
IV. Конкурс эрудитов
[-точность ответа; -скорость ответа; -качество выполнения; -соблюдение правил техники безопасности при выполнении опытов]
|
|
Задания-баллы Оценка
1зад – 3 балла _____
2 зад – 5баллов _____
3 зад –5 баллов _____
|
Задания-баллы Оценка
1зад – 3 балла _____
2 зад – 5 баллов _____
3 зад – 5 баллов _____
|
Задания-баллы Оценка
1зад – 3 балла _____
2 зад – 5баллов _____
3 зад – 5баллов _____
|
|
V. Проверь себя (оценивается учителем после урока)
[-знание химических свойств; -правильность написания уравнений химических реакций] – оценивается отдельно каждый ученик.
|
|
Это интересно знать (3 балла)
[- точность ответа; -оригинальность собственных ответов; -использование дополнительных источников]
|
|
|
|
|
|
VI. Дисциплина участников (1 балл)
[-поведение по отношению к соперникам и членам жюри; -соблюдение правил проведения конкурсов]
|
|
|
|
|
|
Окончательное количество баллов
|
|
|
|
|
| |
|
|
|
|